La tabla periódica es un sistema de distribución y organización de los elementos químicos desarrollada por Dimitri Ivánovich Mendeléiev en 1869. La creación de un sistema como este había sido tema de estudio durante todo el siglo XIX y otros científicos como Antoine Lavoisier, Johan Dobereiner o John Newlands ya habían planteado modelos previos que terminaron por ser descartados por un motivo u otro. El planteamiento de Mendeléiev se convirtió en una revolución para el mundo de la química.
El científico ruso consiguió distribuir los elementos conocidos de forma que siguieran un orden creciente respecto a su peso atómico y al mismo tiempo estuvieran agrupados según características o propiedades similares siguiendo un patrón periódico (de ahí le viene el nombre).
Estas semejanzas se producen entre los distintos elementos que se encuentran en la misma columna y eso permitía predecir las propiedades de elementos que aún no habían sido descubiertos y para los que Mendeléiev dejó huecos en blanco que fueron rellenándose con el paso del tiempo.
Te interesa: ¿Te has preguntado por qué dormimos?
Su nueva ley periódica se dio a conocer frente a la Sociedad Rusa de Química en marzo de 1869 afirmando que "los elementos se agrupaban de acuerdo al valor de su peso atómico y presentaban una clara periodicidad en sus propiedades".
Este primer diseño incluía los 70 elementos químicos conocidos entonces y ganó popularidad tras el descubrimiento del galio, el escandio y el germanio, elementos que se habían predicho en el modelo del químico ruso. A pesar del hito que supuso, Mendeléiev perdió la oportunidad de ganar el Nobel de Química en 1906 y murió poco tiempo después.
En 1913 el químico inglés Henry Moseley determinó, mediante el uso de rayos X, la carga nuclear de los elementos y decidió replantear el diseño de 1869 ordenando los elementos en función de su número atómico (el número de protones que tiene cada átomo de ese elemento) de forma creciente.
El hecho de que el lugar de numerosos elementos siguiera siendo el mismo demuestra el buen juicio de Mendeléiev a la hora de elegir los criterios para su tabla.
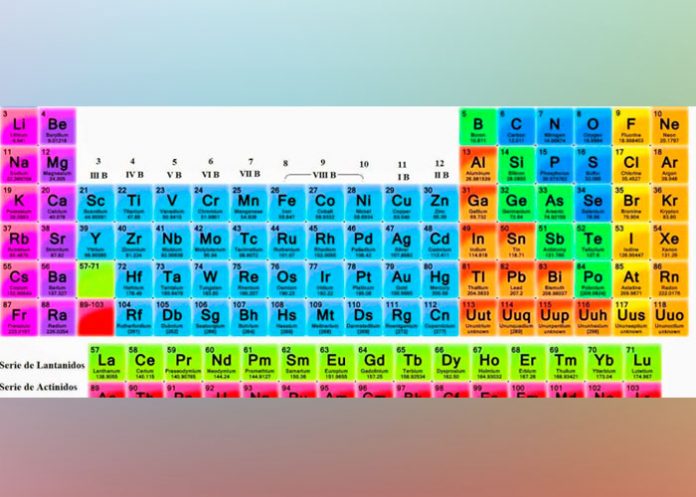
En la actualidad se sigue utilizando el modelo de Moseley, que cuenta con 118 elementos químicos distribuidos en 7 filas y 19 columnas, además de los lantánidos y actínidos. Los elementos se agrupan entre metales (en el lado izquierdo de la tabla), no metales y semimetales.
En cada puesto de la tabla, además del nombre y la abreviatura del elemento, se muestra su número atómico en función del cual se han distribuido, sus electrones de valencia (electrones de la última capa que determinan las propiedades y reactividad de los elementos) y, en muchos casos, su peso atómico.